Lungenkrebs

Gehe zu...
- Lungenkrebs (Bronchialkarzinom, Lungenkarzinom)
- Das Wichtigste über Lungenkrebs in Kürze
- Was ist Lungenkrebs?
- Welche Anzeichen und Symptome gibt es bei Lungenkrebs?
- Welche Ursachen hat Lungenkrebs?
- Wie wird Lungenkrebs diagnostiziert?
- Krankheitsstadien und Verlauf bei Lungenkrebs
- Lebenserwartung und Heilungschance bei Lungenkrebs
- Wie wird Lungenkrebs therapiert?
- Leben mit Lungenkrebs
Lungenkrebs (Bronchialkarzinom, Lungenkarzinom)
Lungenkrebs – in der Fachsprache auch Lungen- oder Bronchialkarzinom genannt – umfasst bösartige (maligne) Tumoren, die aus Lungengewebe entstehen.1 Sie schädigen das Lungengewebe und schränken die überlebenswichtige Funktion der Lunge ein.
Themen im Überblick:
➤ Das Wichtigste über Lungenkrebs in Kürze
➤ Was ist Lungenkrebs?
➤ Welche Anzeichen und Symptome gibt es bei Lungenkrebs?
➤ Welche Ursachen hat Lungenkrebs?
➤ Wie wird Lungenkrebs diagnostiziert?
➤ Krankheitsstadien und Verlauf bei Lungenkrebs
➤ Lebenserwartung und Heilungschancen
➤ Wie wird Lungenkrebs therapiert?
➤ Leben mit Lungenkrebs
Das Wichtigste über Lungenkrebs in Kürze
In Deutschland ist Lungenkrebs bei Männern die zweit- und bei Frauen die dritthäufigste Krebsart – weltweit sogar die häufigste.23 Jedes Jahr erhalten deutschlandweit ca 35.000 Männer und 22.000 Frauen die Diagnose „Lungenkrebs“. Das mittlere Erkrankungsalter liegt dabei bei ca. 70 Jahren.2 Doch was genau ist Lungenkrebs? Expert:innen unterscheiden beim Lungenkarzinom zwischen zwei Formen:1
- Kleinzelliger Lungenkrebs (small cell lung cancer, SCLC)
- Nicht-kleinzelliger Lungenkrebs (non small cell lung cancer, NSCLC)
Die beiden Formen unterscheiden sich in ihrem Verlauf und den Behandlungsmöglichkeiten. Hier erfahren Sie viel Wissenswertes über den nicht-kleinzelligen Lungenkrebs (NSCLC), welcher mit ca. 85 Prozent der diagnostizierten Fälle die häufigste Form von Lungenkrebs ist.1
Was ist Lungenkrebs?
Die Lunge
Die Lunge besteht aus zwei Lungenflügeln, welche wiederum aus Lungenlappen bestehen – der linke aus zwei und der rechte aus drei. In der Struktur ähnelt die Lunge einem Baum: Von der Luftröhre (Trachea) gehen die Hauptbronchien (große Äste) ab, die sich in der Lunge weiter in kleinere Bronchien (kleine Äste) und Bronchiolen (Zweige) verzweigen. Am Ende der kleinsten Bronchiolen sitzen insgesamt etwa 300 Millionen Lungenbläschen (Alveolen ≙ Blätter), in denen der Gasaustausch stattfindet.4 Beim Einatmen nehmen wir Sauerstoff auf und geben Kohlenstoffdioxid beim Ausatmen wieder ab.

Unser Körper besteht aus Milliarden von Zellen, die sich teilen, um alte Zellen durch neue Zellen zu ersetzen. Dabei sorgt unser Körper dafür, dass Zellen sich nicht unkontrolliert vermehren. Bestimmte Faktoren können jedoch das Erbgut schädigen und so eine gesunde Körperzelle in eine Krebszelle verwandeln. Krebszellen sprechen oft nicht mehr auf die Signale des Körpers wie beispielsweise Stopp-Signale bei der Zellteilung an und vermehren sich dann unkontrolliert: Es entsteht ein Tumor. Zudem können Krebszellen in benachbartes Gewebe eindringen und sich so – über die Blut- und Lymphbahnen sogar im gesamten Körper – verbreiten, wodurch Metastasen entstehen können. Metastasen sind Tochtergeschwülste, die sich an anderen Körperstellen durch wandernde Tumorzellen bilden können.
Welche Anzeichen und Symptome gibt es bei Lungenkrebs?
Wie bei vielen Krebserkrankungen, so sind auch bei Lungenkrebs die Anzeichen der Erkrankung (Symptome) nicht immer eindeutig. Es gibt Symptome, die auf den Tumor in der Lunge zurückzuführen sind, sowie Metastasen-bedingte Symptome, die durch Tochtergeschwülste des Tumors (Metastasen) in anderen Körperregionen entstehen.
Folgende Beschwerden können unter anderem bei einem Lungenkarzinom auftreten – doch nicht jedes dieser Symptome deutet zwangsläufig auf einen Tumor hin:15678
- Langanhaltender Husten
- Blutiger Auswurf (Bluthusten oder Bluterbrechen)
- Atem-/Luftnot, Kurzatmigkeit und pfeifende Atemgeräusche
- Schmerzen in der Brust
- Schluckbeschwerden, Halsschmerzen, Heiserkeit ohne Erkältung
- Wiederkehrende Atemwegsinfekte
- Allgemeiner Kräfteverlust und Schwächegefühl
- B-Symptome: ungewollter Gewichtsverlust, Appetitlosigkeit, Fieber und Nachtschweiß
- Trommelschlegelfinger (eine Verdickung der Fingerspitzen), stark gewölbte Fingernägel (Uhrglasnägel)
Mögliche Metastasen-bedingte Symptome können unter anderem folgende sein:15679
- Schwellung der Lymphknoten (bei Lymphknotenmetastasen)
- Schwindel, Gleichgewichtsstörungen, Verwirrtheit, Krampfanfälle, Lähmungen, Kopfschmerzen sowie Wesensveränderungen (bei Hirnmetastasen)
- Gelbsucht (Gelbfärbung von Haut und Augäpfeln) oder Juckreiz (bei Lebermetastasen)
- Knochenschmerzen oder Brüche (bei Knochenmetastasen)
- Rücken- oder Bauchschmerzen, Blutungen oder Unterfunktion der Nebennieren (bei Nebennierenmetastasen)
- Pleuraerguss (Flüssigkeit/Wasser zwischen Lungen- und Rippenfell)
Zu Beginn verläuft die Erkrankung oft beschwerdefrei und zehn Prozent der Patient:innen weisen bei der Diagnose keine Symptome auf. Dies führt dazu, dass Lungenkrebs oft erst spät entdeckt wird.510 Eine Diagnose in einem frühen Stadium der Erkrankung ist meist Zufall – etwa 80 Prozent der Patienten erhalten ihre Diagnose erst im fortgeschrittenen oder metastasierten Stadium.10 Je früher das Bronchialkarzinom diagnostiziert wird, desto besser lässt es sich behandeln.
Unsere Expert:innen bei Lungenkrebs

Onkologie / Hämatologie
Als Experte in den Fachbereichen Onkologie und Hämatologie beantwortet Herr Prof. Dr. Dr. Müller Ihre Fragen rund um die Krebserkrankungen.
Lesen Sie hier die Fragen, die andere Betroffene bereits rund um Onkologie und Hämatologie an Prof. Dr. Müller gestellt haben.
EM-158938

Psychoonkologie
Als Expertin im Bereich Psychoonkologie beantwortet Frau Dr. Meger-David Ihre Fragen rund um die Psyche und Krebs bzw. beim Verstehen und Bewältigen einer Krebserkrankung.
Lesen Sie hier die Fragen, die andere Betroffene bereits rund um Psychoonkologie an Dr. Meger-David gestellt haben.
EM-158936
Welche Ursachen hat Lungenkrebs?
Es gibt Risikofaktoren, welche die Entstehung von Lungenkrebs begünstigen können. Sie werden in erworben und genetisch unterteilt. Erworbene Risikofaktoren entstehen durch äußere Einflüsse, die Körperzellen schädigen und zu Erbgutveränderungen (Mutationen) führen können.15 Dazu gehören beispielsweise:
- Rauchen (auch Passivrauchen)
- Berufliche Einflüsse (Kontakt mit krebserregenden Substanzen wie zum Beispiel Arsen, Asbest, Polyzyklische aromatische Kohlenwasserstoffe (PAK), Quarzstäube, Cadmium oder Chrom in der Bau- und Chemieindustrie, im Bergbau, in KFZ-Schlossereien und Lackierereien)
- Hohe Schadstoffbelastung (Asbest, Feinstaub und Abgase)
- Strahlenbelastung (Röntgen oder natürliches Radon)
- Chronische Infektion der Lunge
Das bedeutet aber nicht, dass Sie zwangsläufig an Lungenkrebs erkranken, wenn Sie einem oder mehreren der Risikofaktoren ausgesetzt sind. Zudem können eine Änderung des Lebensstils (sportliche Betätigung sowie ausgewogene, gesunde Ernährung) oder bestimmte Schutzmaßnahmen bei der Arbeit das Risiko für eine Erkrankung minimieren.1 Aber auch, wenn Sie vollkommen gesund leben, kann Lungenkrebs durch eine Erbgutveränderung auftreten, wenn bei der Verdopplung der DNA vor der Zellteilung ein Fehler auftritt, der nicht korrigiert wird. Aufgrund der genetischen Vorbelastung haben Kinder, deren Eltern an Lungenkrebs erkrankt sind, ein doppelt so hohes Risiko selbst zu erkranken wie Kinder, in deren Familie kein Bronchialkarzinom aufgetreten ist.11
Lungenkrebs kann sowohl durch erworbene Risikofaktoren als auch durch genetische Faktoren verursacht werden.
Wie wird Lungenkrebs diagnostiziert?
Achten Sie auf mögliche Anzeichen, die Ihnen ungewöhnlich vorkommen und auf ein Lungenkarzinom hinweisen können. Denn je früher ein Lungenkarzinom erkannt wird, desto besser ist es behandelbar. Dabei kommen verschiedene Diagnoseverfahren zum Einsatz. Ziel ist es, den Tumor möglichst genau zu bestimmen, um die beste Therapie festlegen zu können.
Folgende Untersuchungen kann der Arzt oder die Ärztin als erstes durchführen:5
- Anamnese und körperliche Untersuchung
- Blutuntersuchung, Blutwerte
- Bildgebende Verfahren (CT, PET-CT, Röntgen, Ultraschall, MRT)
- Histologische Untersuchungen (z.B. Bronchoskopie zur Biopsiesicherung)
- Molekularbiologische Untersuchungen (Sequenzierung)
- Immunhistologische Untersuchungen (Immunoassays)
Eine gute und zuverlässige Diagnostik ist essenziell und benötigt eine gewisse Zeit. Bei der Computertomografie erhalten Sie in der Regel die Ergebnisse innerhalb weniger Tage. Bei Immunhistologischen Untersuchungen kann es ein paar Tage und bei einer molekularbiologischen Untersuchung je nach Testmethode bis zu zwei Wochen dauern. Wenn Sie Fragen zu den diagnostischen Verfahren oder zu den Ergebnissen haben, scheuen Sie sich nicht, diese Ihrem Arzt oder Ihrer Ärztin oder dem Behandlungsteam zu stellen. Je besser Sie Ihre Erkrankung verstehen, desto stärker können Sie sich bei den anstehenden Entscheidungen mit einbringen.
Begleitpersonen
Nehmen Sie zu den Arztgesprächen eine Begleitperson mit – vier Ohren hören mehr als zwei. Das geht auch über Telefon oder Videoanruf. Notieren Sie sich Ihre Fragen vorher und schreiben Sie – oder Ihre Begleitung – die Antworten mit.

Anamnese, körperliche Untersuchung und Blutuntersuchung
Bei einem Verdacht auf Lungenkrebs macht sich Ihr Arzt oder Ihre Ärztin zuerst in einem ausführlichen Gespräch (Anamnese) ein Bild von Ihrer bisherigen Krankheitsgeschichte. Dabei fragt er oder sie Sie beispielsweise nach Ihren Lebensgewohnheiten, potenziellen Risikofaktoren, aktuellen Beschwerden und bestehenden Erkrankungen, wozu auch familiäre Vorerkrankungen gehören.5 Bei der folgenden körperlichen Untersuchung misst der Arzt oder die Ärztin beispielsweise Blutdruck, hört Herz und Lunge ab, kontrolliert die Lymphknoten und tastet den Bauchraum ab. Zusätzlich nimmt der Arzt oder die Ärztin Ihnen Blut für die Laboruntersuchung ab. Aus dem Blutbild und einigen anderen Werten wie Leber- und Nierenwerten können dann Rückschlüsse auf den gesundheitlichen Zustand gezogen werden.5
Bildgebende Verfahren (CT, PET-CT, Röntgen, Ultraschall, MRT)
Es gibt verschiedene bildgebende Verfahren, die bei der Diagnose eines Bronchialkarzinoms zum Einsatz kommen können. Zuerst wird meist mittels Computertomographie (CT) festgestellt, ob ein Tumor in der Lunge vorhanden ist und ob er sich schon in benachbartes Gewebe oder Lymphknoten ausgebreitet hat. Die CT kann auch Bereiche der Lunge darstellen, die von anderen Strukturen des Brustraums überlagert werden und deswegen im Röntgenbild oder beim Ultraschall nicht sichtbar sind. So erhält der Arzt oder die Ärztin genaue Informationen über die Größe, die Lage und die Ausdehnung des Tumors sowie eine mögliche Ausbreitung auf andere Organe. Eine noch exaktere Bestimmung ist mit der Positronen-Emissions-Tomographie-CT (PET-CT) möglich. Alternativ dazu kann eine Magnetresonanztomographie (MRT) eingesetzt werden.15
Histologische Untersuchungen (Lungenspiegelung, Bronchoskopie)
Histologie ist die Lehre von Geweben. Hierbei wird das Tumorgewebe genauer untersucht. Die Gewebeentnahme kann entweder im Rahmen einer Lungenspiegelung (Bronchoskopie) oder einer transthorakalen (durch den Brustkorb hindurch) Punktion gewonnen werden. Dabei werden Gewebeproben aus der Lunge und dem Tumor entnommen und dann unter dem Mikroskop untersucht. Bei der Lungenspiegelung führt der Arzt oder die Ärztin einen biegsamen dünnen Schlauch durch den Mund oder die Nase über die Luftröhre bis in die Lunge, um Gewebeproben oder Zellen durch eine Spülung (Lungenlavage) oder einen Bürstenabstrich zu entnehmen. Auf diese Weise kann zum Beispiel festgestellt werden, ob der Tumor gut- oder bösartig ist. Die Lungenspiegelung ist die wichtigste Methode zur Diagnosesicherung.5 Kann bei einer Lungenspiegelung kein Gewebe gewonnen werden, entnimmt der Arzt oder die Ärztin Gewebeproben durch eine transthorakale Punktion. Dabei wird das Gewebe mithilfe einer dünnen Nadel (Feinnadelbiopsie) gewonnen, zum Beispiel vom Tumor oder aus den Lymphknoten. Eine besondere Form der Biopsie ist die Mediastinoskopie, welche Proben aus den Lymphknoten im Raum zwischen den Lungenflügeln entnimmt. Dadurch kann der Arzt oder die Ärztin unter anderem das Tumorstadium bestimmen oder erkennen, ob die Lymphknoten schon befallen sind.15
Warum ist der Arzt oder die Ärztin besonders an den Lymphknoten interessiert?
Sie sind für die Bestimmung des Stadiums und die anschließende Behandlung von großer Bedeutung. Denn von den Lymphknoten aus können sich Tumorzellen leicht im restlichen Körper verteilen. Deswegen ist es wichtig, genau zu untersuchen, ob und in welchem Ausmaß sie betroffen sind.

Eine Untersuchungsmethode, die keinen Eingriff erfordert, ist die Untersuchung des Auswurfs (Sputum). Dabei wird der Auswurf analysiert, der beim Husten abgegeben wird. Er enthält Zellen der Schleimhaut aus den Bronchien oder anderen Teilen der Lunge, welche dann untersucht werden können. Diese Methode ist allerdings nicht besonders aussagekräftig.5
Anhand der histologischen Eigenschaften lässt sich der NSCLC in vier Unterformen unterteilen:1
- Adenokarzinom (entsteht aus den Zellen des Drüsengewebes der Lunge)
- Plattenepithelkarzinom (entsteht aus den Schleimhautzellen im Bereich der Bronchien)
- Großzelliges Karzinom (wenn weder ein Adeno- noch ein Plattenepithelkarzinom vorliegt)
- Sonstige nicht-kleinzellige Lungenkarzinome
Molekularbiologische Untersuchungen (Treibermutationen)
Eine Krebserkrankung entsteht durch Veränderungen im Erbgut. Diese können das Zellwachstum anregen und dafür sorgen, dass sich Tumorzellen unbegrenzt teilen. Zusammengefasst werden diese genetischen Veränderungen in den Lungenkrebszellen als Treibermutationen bezeichnet.12 Es sind zahlreiche solcher Mutationen bekannt. Die häufigsten bei Lungenkrebs sind: KRAS-Mutation, EGFR-Mutation, ALK-Translokationen, BRAF-Mutation, ROS1-Translokationen, NTRK-Fusion, MET-Amplifikation, RET-Fusion und HER2-Mutation.112 Welche Veränderungen genau vorliegen, kann von Patient:in zu Patient:in sehr verschieden sein und hat einen großen Einfluss auf die Wahl und Wirksamkeit der Therapie. Sie dienen als Biomarker und geben Hinweise darauf, welche Therapie den bestmöglichen Erfolg erzielen kann.13
Warum ist eine frühe Testung so wichtig?
Treibermutationen treten abhängig von der Art des NSCLC unterschiedlich häufig auf. Während diese beim großzelligen Karzinom in der Regel nicht nachgewiesen werden können, können sie beim Plattenepithelkarzinom bei 5-10 % der Betroffenen und beim Adenokarzinom sogar bei fast jeder/jedem zweiten Betroffenen gefunden werden.12
Molekularbiologische Tests zum Nachweis solcher Treibermutationen sind wichtig für die Wahl der bestmöglichen Behandlung. Diese sollten daher schon bei Erstdiagnose, spätestens aber bei einer fortgeschrittenen Erkrankung durchgeführt werden.14
Frag dein Behandlungsteam nach deiner Diagnose deshalb unbedingt nach einer solchen Testung, um die für dich beste Therapie zu finden.

Alles was Sie zur Biomarker-Testung wissen müssen, finden Sie in unserem Leitfaden. Treffen Sie durchdachte Entscheidung zu Ihrer Behandlung mithilfe unserer Broschüre.

Eine Biomarker-Testung bei Lungenkarzinom ist wichtig für eine personalisierte Behandlung. Unsere Checkliste enthält wichtige Fragen für Ihr Behandlungsteam. Laden Sie die Liste herunter und ergänzen Sie eigene Fragen. So sind Sie bestens vorbereitet und können in einem Beratungsgespräch die optimale Therapie planen.
Verschiedene Treibermutationen bei Lungenkrebs:1215

KRAS-Mutation
Ein mutiertes KRAS-Gen schaltet den EGFR-Wachstumsweg (epidermaler Wachstumsfaktor-Rezeptor) permanent ein, wodurch es zu einer unkontrollierten Zellteilung kommt. Diese Mutation tritt vor allem bei langjährigen Rauchern auf. Ca. 25% der NSCLC-Patient:innen weisen eine KRAS-Mutation auf.1216
EGFR-Mutation
Die Abkürzung EGFR stammt aus dem Englischen und bedeutet übersetzt "epidermaler Wachstumsfaktor-Rezeptor". Bindet ein Wachstumsfaktor an den Rezeptor wird die Zellteilung eingeleitet. Eine Mutation dieses Rezeptors kann dazu führen, dass dieser dauerhaft aktiviert wird, wodurch eine unkontrollierte Zellteilung stattfindet. Eine EGFR-Mutation tritt besonders häufig bei Frauen und Nichtrauchern auf. Insgesamt sind ca. 10% aller NSCLC-Patient:innen von dieser Mutation betroffen. Zielgerichtete Medikamente können dem unkontrolliertem Tumorwachstum entgegenwirken, indem sie den mutierten EGFR blockieren und verhindern, dass weiter Wachstumssignale ausgesendet werden.17
ALK-Translokation
Das ALK-Gen liefert den Bauplan für das Protein anaplastische Lymphomkinase (ALK). Kommt es bei diesem Gen zu einer Verlagerung bestimmter Genabschnitte an eine andere Position (Translokation), führt dies zu einer dauerhaften Aktivierung der ALK, wodurch das unkontrollierte Wachstum des Tumors gefördert wird. Etwa 3-5% der NSCLC-Patient:innen sind ALK-positiv. Besonders jüngere Patient:innen und Nieraucher sind von dieser genetischen Veränderung betroffen.1217
BRAF-Mutation
Hierbei liegt eine Mutation im BRAF-Gen vor, welche die BRAF Serin-Threonin-Kinase dauerhaft aktiviert und so zu einer übermäßigen Vermehrung der Tumorzellen führt. Diese Mutation liegt bei ca. 2-4% der NSCLC-Patient:innen vor.18
MET-Amplifikationen
Die MET-Tyrosinkinase steuert Signalwege, die das Zellwachstum und die Zellvermehrung regulieren. Durch die Vervielfältigung (Amplifikation) des Gens kommt es zu einer Überfunktion der MET-Tyrosinkinase, was zu einem unkontrolliertem Zellwachstum führt. Diese MET-Amplifikationen können als primäre Treibermutation (d.h. ohne andere Treibermutationen) vorkommen oder als Resistenzmechanismus bei Behandlung mit anderen Kinasehemmern (z.B. EGFR-Hemmern). Bei ca. 2-5% der NSCLC-Patient:innen treten die MET-Amplifikationen als primäre Treibermutation auf.1219
RET-Fusionen
Die RET-Tyrosinkinase steuert Signalwege, die das Zellwachstum und die Zellvermehrung regulieren. Veränderungen des RET-Gens können zu einer Verschmelzung (Fusion) der RET-Tyrosinkinase mit anderen Proteinen führen, wodurch die RET-Tyrosinkinase dauerhaft aktiviert wird. Diese ständige Aktivierung von RET ermöglicht den Tumorzellen ein unkontrolliertes Wachstum. Bei ca. 1-2% der NSCLC-Patient:innen wird eine RET-Fusion als Treibermutation festgestellt.20
ROS1-Translokation
Veränderungen im ROS1-Gen bewirken ebenfalls eine übermäßige Vermehrung der Tumorzellen. Diese Translokation kommt bei ca. 1-2% der NSCLC-Patient:innen vor und tritt gehäuft bei jüngeren Patient:innen und Nierauchern auf.21
HER2-Mutation
HER2 (Humaner epidermaler Wachstumsfaktor Rezeptor 2) ist ein Tyrosinkinase-Rezeptor und reguliert das Zellwachstum und die Zellvermehrung. Bei ca. 3% der NSCLC-Patient:innen treten Mutationen im HER2-Gen auf, wodurch es zu einer Überaktivierung der Tyrosinkinase kommt. Diese führt zu unkontrolliertem Zellwachstum und -vermehrung der Tumorzellen.22
NTRK-Fusion
Durch Umlagerungen von Genabschnitten der NTRK-Gene an eine andere Position (Translokation), kann es zu einer ungeplanten Verschmelzung (Fusion) zweier Proteine kommen. Diese Fusionsproteine können das Tumorwachstum fördern. Diese NTRK-Fusionen kommen bei weniger als 1% der NSCLC-Patient:innen vor.23
Doch wie werden solche Treibermutationen bestimmt? Dafür wird eine genetische Untersuchung durchgeführt. Aus der durch eine Biopsie gewonnenen Tumorprobe wird die DNA der Zellen isoliert und auf Veränderungen untersucht. Hierbei kommt besonders das Next-Generation-Sequencing (NGS) zum Einsatz. Mit seiner Hilfe können die DNA-Proben in einer hohen Geschwindigkeit und mit hoher Genauigkeit analysiert werden. So kann das Erbgut – im Gegensatz zu früher – auf mehrere Mutationen gleichzeitig untersucht werden.24
Alternativ zur herkömmlichen Biopsie kann die Tumor-DNA auch aus dem Blut der betroffenen Person gewonnen werden. Diese moderne Methode nennt man Flüssigbiopsie (Liquid Biopsy) – sie kann bereits winzige Mengen an Tumorerbgut im Blut nachweisen. Sie wird jedoch nicht bei der Erstdiagnose eingesetzt, sondern erst im Verlauf der Erkrankung.
Immunhistologische Untersuchungen (Biomarker, Tumormarker)
Durch eine immunhistologische Untersuchung können noch andere Tumor-/Biomarker bestimmt werden, die eine wichtige Rolle für die Therapieentscheidung spielen. Bei Lungenkrebs ist das beispielsweise PD-L1. PD-L1 (Programmed Death-Ligand 1) ist ein sogenannter Immun-Checkpoint – ein Kontrollpunkt des Immunsystems. Diese Strukturen können auf der Oberfläche von Tumorzellen vorhanden sein und schützen diese vor einem Angriff des Immunsystems, sodass die Krebszelle ungehindert weiterwachsen und sich vermehren kann. Hier setzen neue Medikamente an, die PD-L1 blockieren und damit die Krebszelle angreifbar für das Immunsystem machen. Das Vorhandensein von PD-L1 auf der Krebsoberfläche bietet einen guten Angriffspunkt für eine Immuntherapie.25

Die Broschüre bietet Betroffenen und ihren Angehörigen umfangreiche Informationen zum nicht-kleinzelligen Lungenkarzinom (NSCLC). Je besser Sie Ihre Erkrankung verstehen, desto einfacher können Sie Ihren ganz persönlichen Umgang damit finden und eine aktive und selbststimmte Rolle einnehmen. Diese Broschüre ist dafür ein guter erster Schritt.

Die Diagnose „Lungenkrebs" wirft vermutlich auch bei Ihnen viele Fragen auf – Fragen, die Sie im nächsten Beratungsgespräch stellen können. Damit Sie keine vergessen, notieren Sie diese am besten direkt. Hier finden Sie eine Checkliste mit Fragen, die auch für Sie interessant sein können. Sie können sich die Liste herunterladen und auch eigene Fragen ergänzen.
Krankheitsstadien und Verlauf bei Lungenkrebs
Die Einteilung des NSCLC in Stadien dient dazu, genau festzulegen, wie weit der Krebs fortgeschritten ist. Neben der Lage und Größe des Tumors spielt es eine bedeutende Rolle, ob der Krebs bereits Lymphknoten befallen oder Metastasen in anderen Organen (Fernmetastasen) gebildet hat. Diese Einteilung fließt ebenfalls in die Entscheidung mit ein, welche Therapie am besten geeignet ist.
Lungenkrebs lässt sich anhand der sogenannten TNM-Klassifikation einteilen:15
Kategorie | Beschreibung |
|---|---|
Kategorie | Beschreibung |
Kategorie | Beschreibung |
Kategorie | Beschreibung |
Tabelle 1: TNM-Klassifikation
Zudem erfolgt die Stadieneinteilung nach den sogenannten UICC-8-Kriterien.15
Krankheitsstadien bei Lungenkrebs
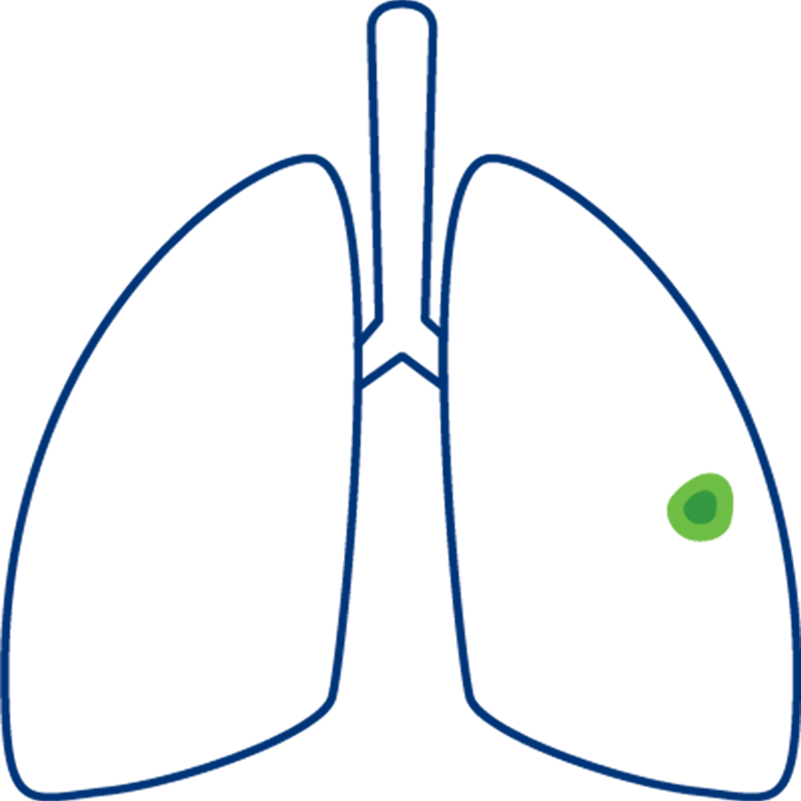
Stadium I
Der Tumor ist auf einen kleinen Bereich in der Lunge begrenzt und es sind weder die Lymphknoten befallen noch Metastasen vorhanden.
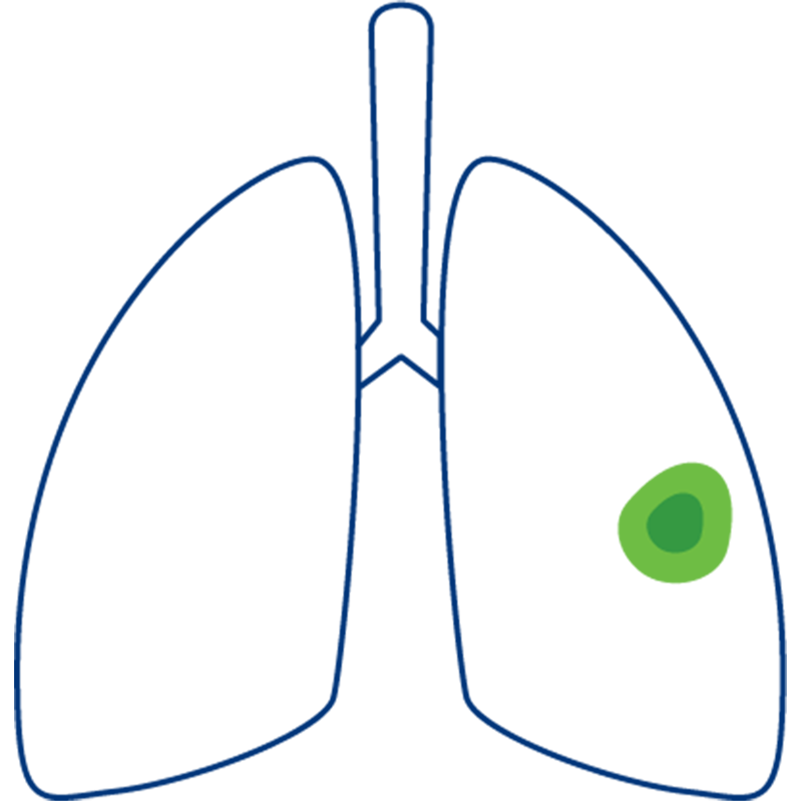
Stadium II
Der Tumor ist noch klein, jedoch sind die umliegenden Lymphknoten bereits befallen.
Oder
Der Tumor ist etwas größer, aber die Lymphknoten sind noch nicht befallen.
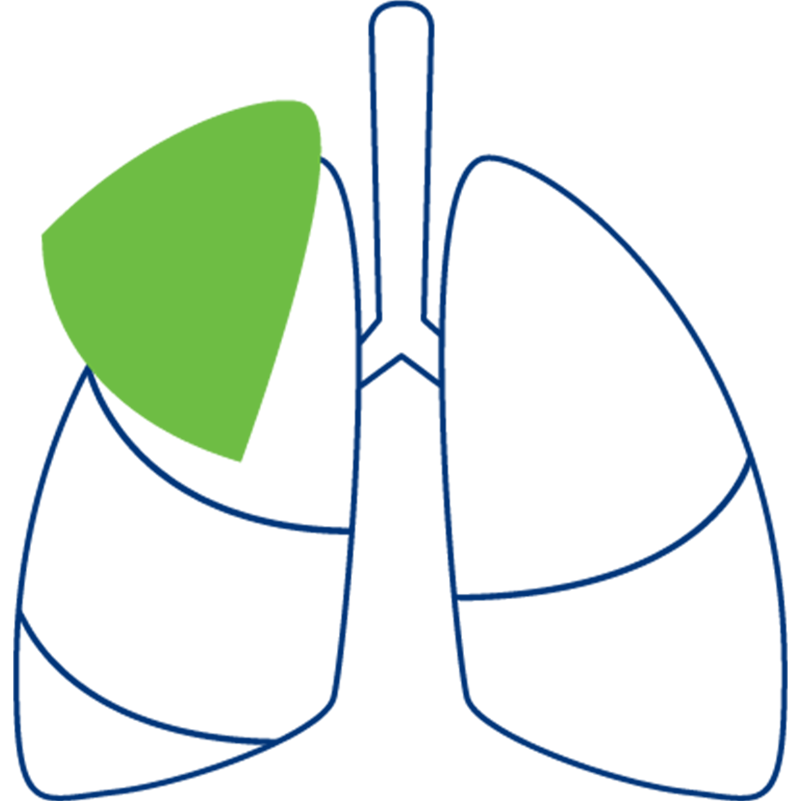
Stadium III
Dieses Stadium umfasst ein sehr verschiedenartiges Krankheitsbild. Der Tumor ist fortgeschritten und hat in die Lymphknoten gestreut.
Oder
Der Tumor ist groß und hat sich in umliegendes Gewebe ausgebreitet, aber noch nicht in die Lymphknoten gestreut.
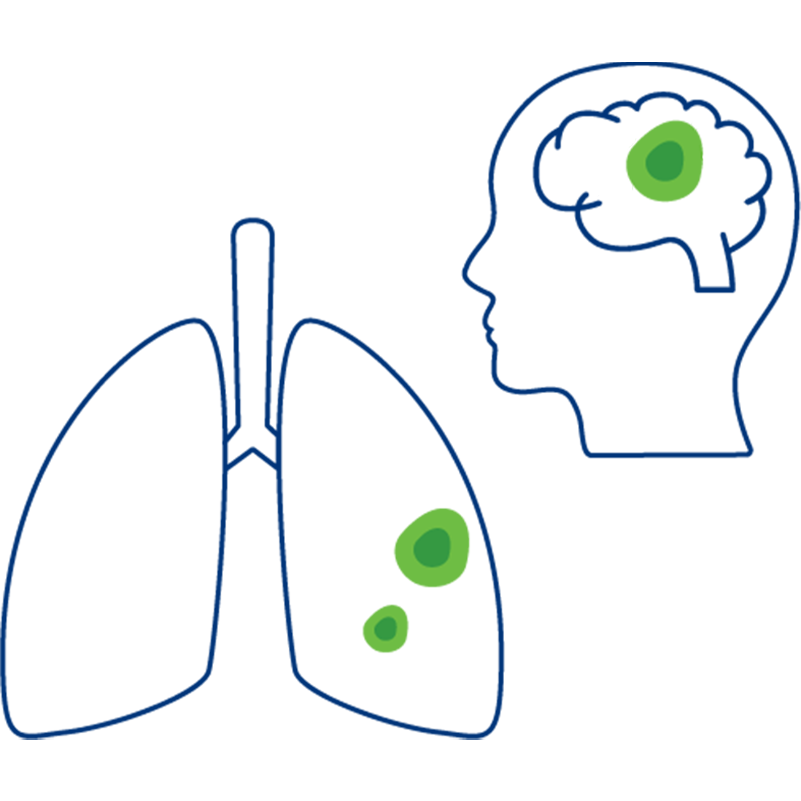
Stadium IV
Stadium 4 wird auch als Endstadium von Lungenkrebs bezeichnet. Der Tumor hat sich über die Lunge hinaus auf andere Körperteile ausgebreitet, also Metastasen gebildet.
Metastasen bei Lungenkrebs
Metastasen treten im fortgeschrittenen Stadium oder auch bei einem wiedergekehrten (rezidiviertem) Lungenkarzinom auf. Dabei können sie in unterschiedlichen Bereichen des Körpers vorkommen. Besonders häufig sind die Lymphknoten, die Knochen, die Leber, die Nebenniere und das Gehirn betroffen. Es können sich aber auch neue Tumoren im gleichen oder im anderen Lungenflügel bilden.1
Mögliche Metastasen-bedingte Symptome können unter anderem folgende sein:15679
- Schwellung der Lymphknoten (bei Lymphknotenmetastasen)
- Schwindel, Gleichgewichtsstörungen, Verwirrtheit, Krampfanfälle, Lähmungen, Kopfschmerzen sowie Wesensveränderungen (bei Hirnmetastasen)
- Gelbsucht (Gelbfärbung von Haut und Augäpfeln) oder Juckreiz (bei Lebermetastasen)
- Knochenschmerzen oder Brüche (bei Knochenmetastasen)
- Rücken- oder Bauchschmerzen, Blutungen oder selten Unterfunktion der Nebennieren (bei Nebennierenmetastasen)
- Pleuraerguss (Flüssigkeit/Wasser zwischen Lungen- und Rippenfell)
Um diese Metastasen zu entdecken, gibt es verschiedene Untersuchungsmöglichkeiten, wie beispielsweise ein MRT, PET-CT oder CT vom Kopf oder von anderen Teilen des Körpers. Eine Ergänzung zur Bestimmung von Knochenmetastasen ist die Knochenszintigraphie.1 Diese Untersuchungen auf Metastasen werden Ausbreitungsdiagnostik genannt.
Gemeinsam forschen gegen Krebs
Zusammen mit dem Bundesministerium für Gesundheit und weiteren Partnern wie die Janssen-Cilag GmbH hat das Bundesministerium für Bildung und Forschung die Nationale Dekade gegen Krebs ausgerufen. Ziel ist es, die Krebsforschung entscheidend voranzubringen und die Heilungschancen zu verbessern – immer mit enger Einbindung der Patient:innen.

Lebenserwartung und Heilungschance bei Lungenkrebs
Die Prognose ist bei jedem:r Patient:in individuell. Sie hängt von Stadium, Genotyp, Histologie, Geschlecht, Allgemeinzustand und eventuellen Komorbiditäten ab. Aufgrund der wachsenden Anzahl und besser werdenden Therapiemöglichkeiten hat sich die Prognose für Lungenkrebs-Patient:innen in den letzten Jahren deutlich verbessert. Die relative 5-Jahres-Überlebensrate liegt bei Männern bei 19 Prozent und bei Frauen bei 25 Prozent.26 Das bedeutet, dass die Chance, fünf Jahre nach der Diagnosestellung noch zu leben, bei Männern durchschnittlich bei 19 Prozent und bei Frauen bei 25 Prozent liegt.26 Je früher ein Lungenkarzinomen entdeckt wird, desto eher kann die Therapie starten und desto besser sind die Heilungschancen.27 In einem fortgeschrittenen Stadium kommt dagegen häufig eine palliative Therapie zum Einsatz.1


In unserem Podcast „MEIN KREBSRATGEBER zum Hören“ lassen wir Betroffene zu Wort kommen, um anderen Mut zu machen. In den Folgen 9, 12 und 13 sprechen Patient:innen und Angehörige über ihren Umgang mit der Lungenkrebserkrankung, Erfahrungen mit der palliativen Behandlung, Bedeutung der Diagnose für das Familienleben und die Lebensqualität bei Lungenkrebs.
Wie wird Lungenkrebs therapiert?
Zur Behandlung stehen zahlreiche Optionen zur Verfügung. Manche Therapien wirken sich auf den ganzen Körper aus (systemisch), andere nur örtlich begrenzt auf den Tumor (lokal oder zielgerichtet). Jedoch gibt es kein Behandlungsschema, das für alle Lungenkrebs-Patient:innen gilt. Denn jeder Krebs ist individuell und welche Therapie für wen infrage kommt, hängt von verschiedenen Faktoren ab. Dazu gehören neben dem gesundheitlichen Allgemeinzustand der erkrankten Person, der Lungenfunktion und dem Vorhandensein von Begleiterkrankungen (Komorbiditäten) auch das Stadium des Bronchialkarzinoms und seine Eigenschaften, beispielsweise welche Mutation vorliegt.15 Aber auch Ihre Wünsche und Vorstellungen werden bei der Therapieentscheidung berücksichtigt. Zusammen mit Ihrem Arzt oder Ihrer Ärztin können Sie so die Therapie auswählen, die am besten zu Ihnen passt. Lassen Sie sich nicht davon beunruhigen, sollte die Diagnostik eine längere Zeit in Anspruch nehmen. Es ist wichtig, den Tumor genau zu kennen, um die für Sie beste Therapie zu finden.
Allgemeinzustand, Lungenfunktion, Komorbiditäten sowie Stadium und Eigenschaften des Tumors bestimmen zusammen mit Ihren Wünschen die eingesetzte Therapie.
Operation
Eine Operation ist – besonders in den frühen Stadien I und II – in der Regel die erste Option zur Behandlung eines Lungenkarzinoms. Abhängig von der Größe und Ausbreitung der Tumorzellen kann aber auch in späteren Stadien noch operiert werden. Ziel der Operation ist, das Tumorgewebe möglichst vollständig zu entfernen. Zusätzlich entnimmt der Arzt oder die Ärztin bei dem Eingriff benachbarte Lymphknoten, um sie im Labor zu untersuchen.15 Es gibt verschiedene Operationsverfahren, die sich nach der Ausdehnung und Größe des Tumors richten.
Die vier häufigsten Operationsmethoden bei Krebs28293031
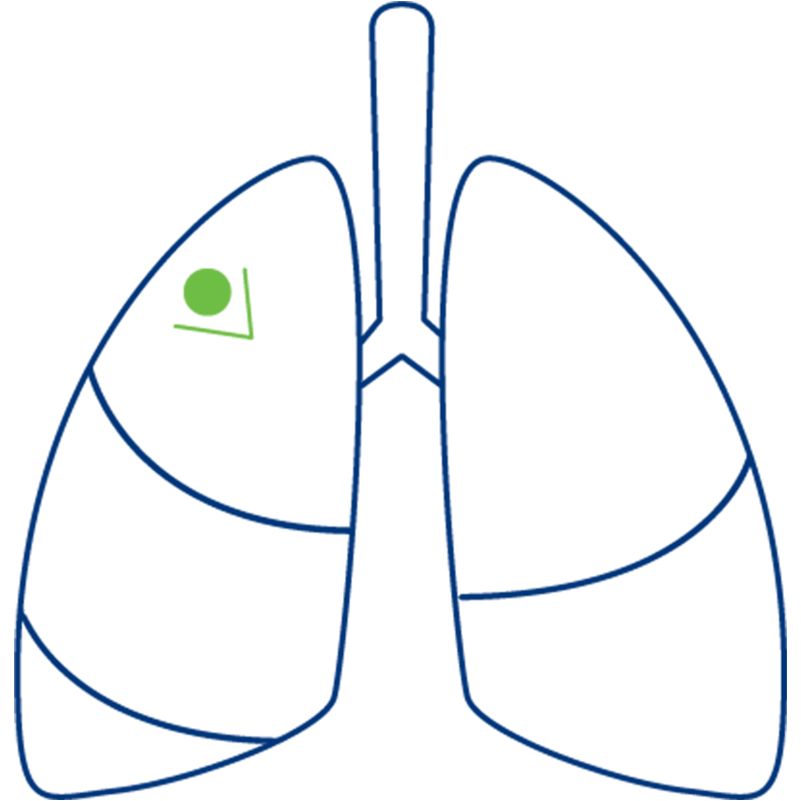
Atypische Resektion (Keilresektion)
Sparsame keilförmige Entfernung des betroffenen Lungengewebes, die nicht dem Aufbau der Lunge folgt; das umliegende gesunde Gewebe bleibt erhalten.
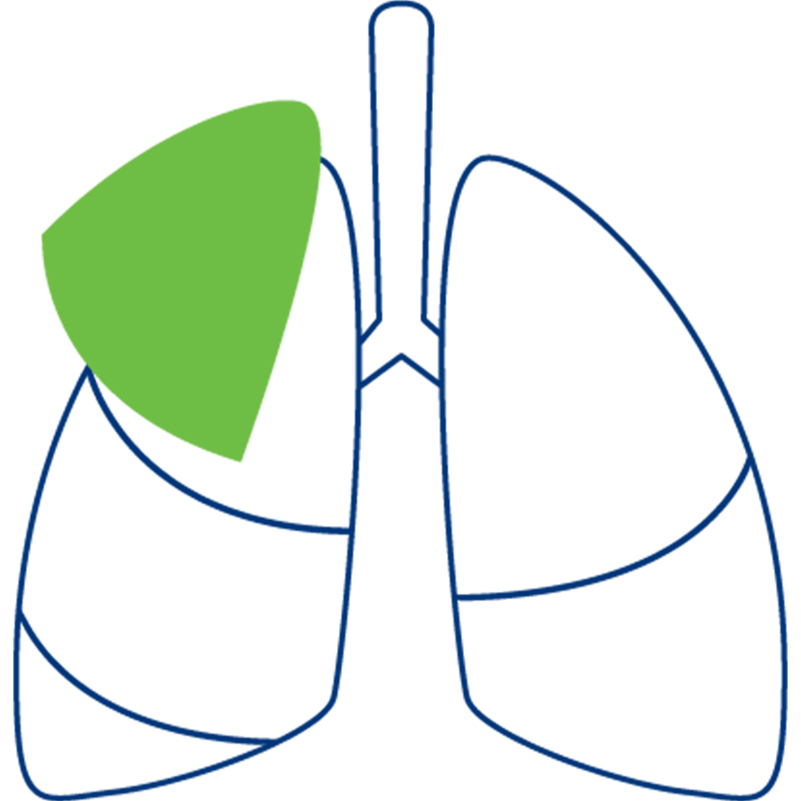
Lobektomie
Vollständige oder teilweise Entfernung eines Lungenlappens; Voraussetzung dafür ist, dass der Tumor auf einen Lungenlappen begrenzt ist.
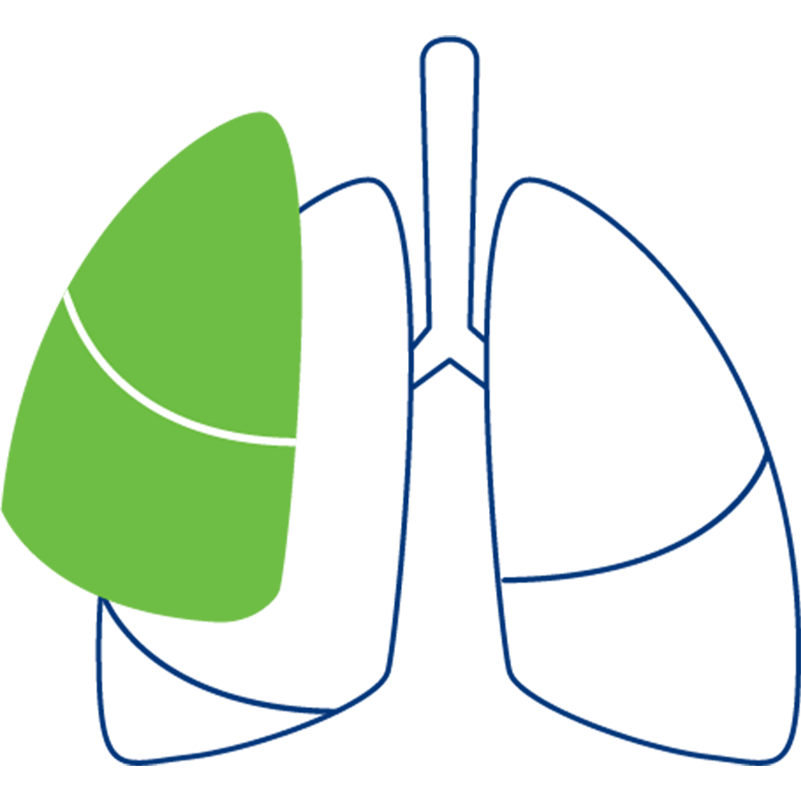
Bilobektomie
Neben dem befallenen wird auch der angrenzende Lungenlappen des rechten Lungenflügels entfernt; notwendig, wenn das Tumorwachstum über die Grenze eines Lungenlappens hinausgeht.
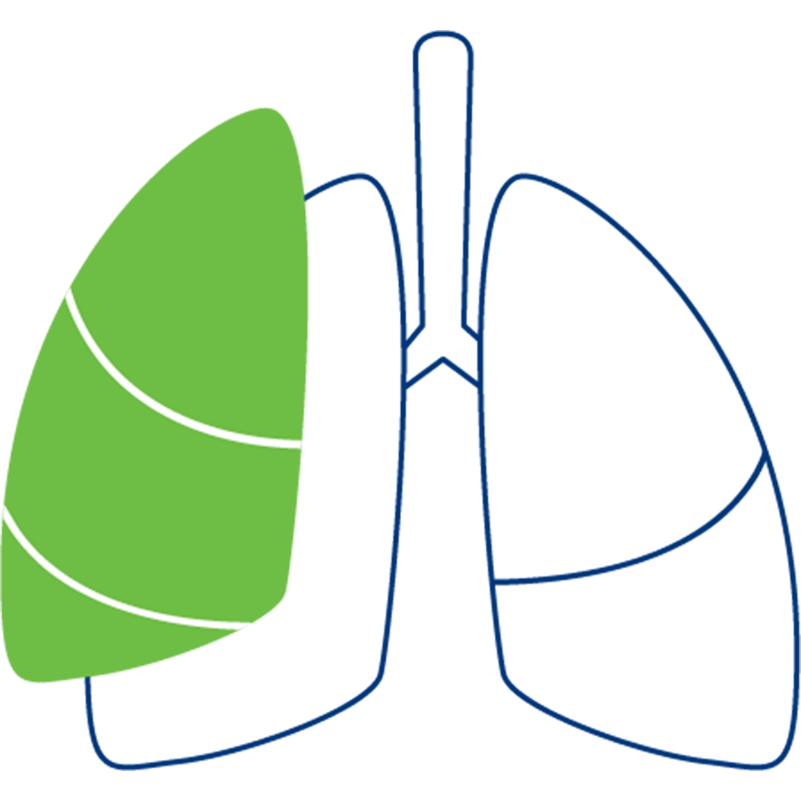
Pneumektomie
Entfernung eines kompletten Lungenflügels aufgrund von beispielsweise großen Tumoren oder mehreren Krebsherden.
Ob eine Operation zur Behandlung geeignet ist, hängt auch von möglichen Vor- oder Begleiterkrankungen ab. Wenn beispielsweise Herzkrankheiten den allgemeinen Gesundheitszustand schwächen, kann das Operationsrisiko zu hoch und eine Strahlentherapie besser geeignet sein. Außerdem muss gewährleistet sein, dass der verbleibende Lungenanteil die Atmung ausreichend übernehmen kann. In manchen Fällen ist es auch erforderlich, den Tumor zuerst durch eine Chemo- oder Strahlentherapie zu verkleinern (neoadjuvante Therapie) und ihn erst dann operativ zu entfernen.15
Die Operation an der Lunge erfolgt unter Vollnarkose und – abhängig von der Lage und Größe des Tumors – minimalinvasiv oder offen. Ein minimalinvasiver Eingriff kommt jedoch nur bei sehr kleinen Tumoren in sehr frühen Stadien vor, daher findet in der Regel eine offene OP statt. Der Arzt oder die Ärztin entfernt das betroffene Gewebe immer mit etwas „Sicherheitsabstand“. Das bedeutet, dass etwas gesundes Gewebe um den Tumor herum zusätzlich entnommen wird, um sicherzustellen, dass keine Tumorzellen zurückbleiben. Falls doch ein paar Tumorzellen in der Lunge geblieben sind, kann eine weitere Operation erforderlich sein.
Nach der Operation muss das verbliebene Lungengewebe die komplette Atemfunktion übernehmen. Aus diesem Grund ist Ihre körperliche Leistungsfähigkeit direkt nach der OP geringer und tiefes Ein- und Ausatmen kann Ihnen schwerfallen. Doch mit einer Rehabilitation und gezielten Atemübungen können Sie Ihre Lungenfunktion wirksam unterstützen. Gegen die Schmerzen nach der Operation können Sie eine Schmerztherapie erhalten.
Strahlentherapie
Eine Strahlentherapie – auch Radiotherapie genannt – kann sowohl ergänzend als auch alternativ zu einer Operation stattfinden. Als neoadjuvante Therapie kann sie vor einer Operation den Tumor verkleinern. Ist eine Operation zum Beispiel aufgrund von weiteren Erkrankungen oder einer stark eingeschränkten Lungenfunktion nicht möglich, kann der Arzt oder die Ärztin eine Bestrahlung des Tumors verordnen. Auch eine Kombination mit einer Chemotherapie ist möglich. Sie kann bei allen Stadien zum Einsatz kommen.15 Doch wie funktioniert eine Strahlentherapie? Die Krebszellen werden energiereicher Strahlung ausgesetzt, welche die DNA der Tumorzellen schädigt und somit das Tumorwachstum hemmt und die Zellen zerstört. Die Strahlentherapie ist zwar eine lokale Therapie – das bedeutet, sie kann gezielt auf den Tumor oder Metastasen gerichtet werden – doch es lässt sich nicht verhindern, dass auch gesunde Körperzellen von den Strahlen geschädigt werden. Diese sind jedoch meist in der Lage, die entstandenen Schäden an der DNA zu reparieren – Krebszellen können das nicht, sterben ab und werden von Immunzellen beseitigt. Das ist der Grund, warum eine Strahlentherapie in mehreren Sitzungen abläuft: In der Zwischenzeit können sich die gesunden Körperzellen regenerieren.32
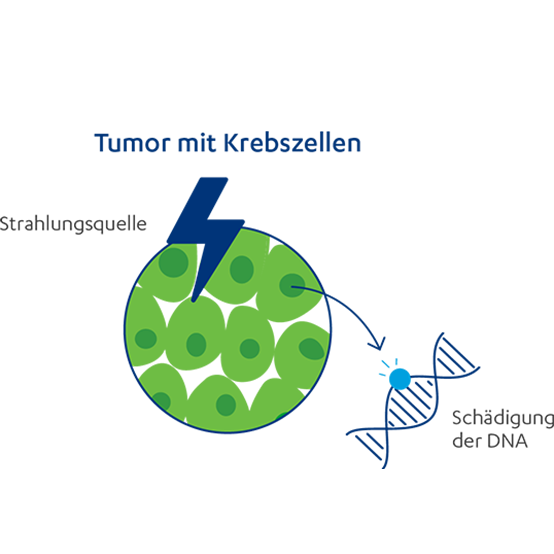


In der Regel ist es möglich, eine Strahlentherapie ambulant durchzuführen. Vor der ersten Bestrahlung bestimmt der Arzt oder die Ärztin die genaue Lage des Tumors im Körper. Mithilfe einer MRT- oder CT-Untersuchung wird die zu bestrahlende Stelle genauestens festgesetzt und auf der Haut der betroffenen Person für die kommenden Sitzungen markiert. Die Bestrahlung an sich dauert meist nur wenige Minuten und ist nicht spürbar.
Eine besondere Form der Bestrahlung ist die Brachytherapie, bei der die Bestrahlung aus nächster Nähe und meist unter Narkose erfolgt. Bei Lungenkrebs schiebt der Arzt/die Ärztin dabei einen sogenannten Applikator, der einen radioaktiven Stoff enthält, durch die Luftröhre zum Tumor. So kann der befallene Lungenbereich direkt behandelt werden. Diese Form der Strahlentherapie kann bei fortgeschrittenen Stadien im Rahmen einer palliativen Behandlung infrage kommen. In selteneren Fällen wird sie auch bei frühen Lungenkrebsstadien eingesetzt, wenn beispielsweise eine Operation nicht möglich ist.33
Ob es bei der Strahlentherapie zu Nebenwirkungen kommt, hängt von den verwendeten Strahlen, der Intensität und der Körperregion ab. Zudem reagiert auch nicht jeder Mensch gleich auf die Bestrahlung. Die meisten Nebenwirkungen entwickeln sich in der Regel nach der Behandlung von allein wieder zurück. Hautveränderungen, wie eine dunkle Verfärbung, können jedoch bleiben.
Bei einer Strahlentherapie können bei Ihnen beispielsweise folgende Begleiterscheinungen auftreten:33
- Müdigkeit sowie anhaltende Erschöpfung (Fatigue)
- Hautreizungen und Hautveränderungen (ähnlich wie bei einem Sonnenbrand), Pigmentflecken auf der Haut
- Haarausfall im bestrahlten Bereich
- Übelkeit und Verdauungsbeschwerden
- Psychische Belastung
- Husten
- Strahlenbedingte Lungenentzündung
Wenn Sie eine oder mehrere dieser Nebenwirkungen bei sich bemerken, informieren Sie Ihr Behandlungsteam. Viele Begleiterscheinungen der Therapie lassen sich medikamentös gut behandeln.
Chemotherapie
Die Chemotherapie ist eine der bekanntesten Behandlungsmethoden für Krebserkrankungen und spielt auch bei Lungenkrebs eine wichtige Rolle. Heutzutage gibt es viele verschiedene Wirkstoffe, die die Zellteilung und somit das Tumorwachstum hemmen. Die Chemotherapie ist bei Lungenkrebs in fast jedem Stadium eine Option – die Ausnahme bildet hier Stadium I. Meist kommt sie zusammen mit anderen Behandlungsmethoden wie einer Strahlentherapie oder einer Operation zum Einsatz. Sie kann auch mit zielgerichteten Therapieformen wie einer Immuntherapie kombiniert werden – dann sprechen Ärzt:innen von einer Immunchemotherapie.15
Neoadjuvant & Adjuvant
Eine Chemotherapie vor einer Operation, die den Tumor verkleinern soll, nennt man in der Fachsprache auch neoadjuvant. Findet die Chemotherapie ergänzend nach einer Operation statt, heißt dies adjuvant.34
Wie wirkt eine Chemotherapie? Die verabreichten Zytostatika (auf Deutsch „Zellhemmer“) verhindern auf unterschiedliche Weise das Wachstum, die Teilung sowie die Vermehrung von Tumorzellen und führen so zu ihrem Absterben. Zellen, die sich besonders häufig teilen, sind dadurch besonders anfällig für eine Chemotherapie. Dazu gehören neben den Krebszellen aber auch gesunde Körperzellen wie beispielsweise Schleimhautzellen, Haarwurzelzellen oder die blutbildenden Zellen im Knochenmark – so kommt es zu den typischen Nebenwirkungen. Doch auch hier können gesunde Körperzellen – im Gegensatz zu den Tumorzellen – die durch die Zytostatika entstandenen Schäden reparieren und die Nebenwirkungen sind meist nicht von Dauer. Für eine ausreichende Erholungszeit der gesunden Zellen wird auch die Chemotherapie in Zyklen verabreicht.34
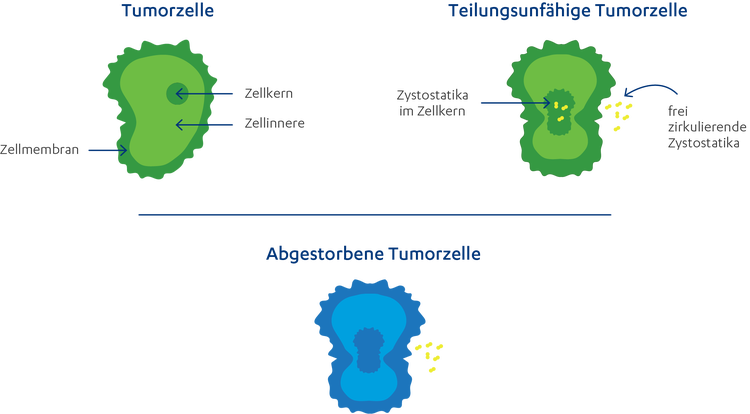
Sie können Zytostatika allein (Monotherapie) oder in Kombination mit anderen Zytostatika oder Therapieformen (Kombinationstherapie) verabreicht bekommen. Sie erhalten eine Chemotherapie als Infusion über die Vene. Dadurch wird das Zytostatikum im gesamten Körper verteilt und wirkt systemisch (auf den ganzen Körper). Daher richtet sie sich auch gegen sehr kleine Absiedlungen von Tumorzellen (Mikrometastasen) und gegen Tochtergeschwüre (Metastasen).34
Eine Chemotherapie läuft in Behandlungszyklen ab: Ein Zyklus umfasst den Tag der Infusion (Tag 1 des Zyklus) mitsamt der nachfolgenden Pause, die meist mehrere Tage lang ist. Je nach Behandlungsschema kann ein Zyklus auch mehrere Infusionen an festgelegten Tagen beinhalten. Wie lang die Zyklen jeweils sind, richtet sich unter anderem nach den angewendeten Medikamenten und dem Gesundheitszustand der erkrankten Person. Daher verteilen sich die Infusionstermine in der Regel über einige Wochen oder Monate. Vor einer Chemotherapie können Sie zusätzliche Medikamente verabreicht bekommen, damit Sie die Chemotherapie besser vertragen. Meist kann die Behandlung ambulant erfolgen, das heißt Sie können nach der Infusion nach Hause gehen und sich von der Behandlung erholen.
Bei der Behandlung von Lungenkrebs kann eine Chemotherapie je nach Stadium unterschiedliche Ziele verfolgen. In frühen Stadien wird eine Heilung der Krebserkrankung angestrebt. Dies nennen Expert:innen eine kurative Therapie. Vor einer Operation kann eine Chemotherapie dafür sorgen, dass der Tumor schrumpft und sich besser entfernen lässt. Nach einer Operation soll sie eventuell verbliebene Krebszellen abtöten, um ein erneutes Tumorwachstum zu verhindern. In fortgeschrittenen Stadien stehen der Erhalt der aktuellen Gesundheitssituation und die Verbesserung der Lebensqualität im Vordergrund. Die Chemotherapie soll das Fortschreiten der Erkrankung verlangsamen. Dabei handelt es sich um eine palliative Therapie.
Welche Nebenwirkungen auftreten und wie stark sie ausgeprägt sind, lässt sich nicht vorhersehen. Sie hängen von den Medikamenten ab und unterscheiden sich auch von Mensch zu Mensch. Die Nebenwirkungen treten also nicht bei jedem auf, der ein bestimmtes Medikament erhält. Heute lassen sich die Nebenwirkungen einer Chemotherapie meist gut behandeln oder vorbeugen.
Bei einer Chemotherapie kann es unter anderem zu folgenden Nebenwirkungen kommen:3435
- Allgemeines Unwohlsein
- Durchfall, Übelkeit und Erbrechen
- Erhöhtes Infektionsrisiko durch eine Schwächung des Immunsystems
- Konzentrationsprobleme und Erschöpfung (Fatigue) sowie Schwäche
- Mangel an Blutzellen
- Mundschleimhautentzündung
- Störungen der Blutgerinnung
- Vorübergehender Haarausfall
Sollten Sie eine oder mehrere dieser Nebenwirkungen bei sich feststellen, informieren Sie Ihr Behandlungsteam. Es kann Ihnen beim Umgang mit den Nebenwirkungen helfen und Ihnen entsprechende Medikamente verabreichen.
Zielgerichtete Therapien
Zielgerichtete Therapien sind besonders im fortgeschrittenen und metastasierten Stadium von großer Bedeutung. Diese Medikamente sind so entwickelt, dass sie mit ganz bestimmten Molekülen wechselwirken, wie beispielsweise Oberflächenmerkmalen auf Krebszellen. Bei Lungenkrebs sind verschiedene Merkmale bekannt, die man mit einer zielgerichteten Therapie angreifen kann. Daher ist bei der Diagnose wichtig, ganz genau zu untersuchen, um welche Lungenkrebsart es sich handelt und ob bestimmte Biomarker oder Erbgutveränderungen/Treibermutationen vorliegen. Wenn ja, lassen sich zielgerichtete Medikamente genau auf die Eigenschaften der Krebszellen abstimmen.36 Allerdings ist nicht jede:r Patient:in für diese Therapieform geeignet. Zu den zielgerichteten Therapien gehören: Immuntherapien, Tyrosinkinase-Inhibitoren, zielgerichtete Antikörpertherapien sowie Angiogenese-Inhibitoren.
Immuntherapie
Die Immuntherapie ist eine moderne, zielgerichtete Behandlungsmethode, die das körpereigene Immunsystem dabei unterstützt, den Krebs zu bekämpfen. Das menschliche Immunsystem bildet die Körperpolizei und ist für die Abwehr von Krankheitserregern wie Viren und Bakterien zuständig. Es erkennt und beseitigt aber auch alte oder krankhaft veränderte körpereigen Zellen wie beispielsweise Krebszellen. Einige Krebszellen können das Immunsystem aber austricksen, indem sie die Abwehrzellen „ausschalten“ und sich so vor dem Immunsystem verstecken. Sie nutzen bestimmte Merkmale auf ihrer Oberfläche, sogenannte Checkpoints, als einen Tarnumhang. Einer dieser Checkpoints ist beispielsweise PD-1/PD-L1. Über diese Checkpoints kommunizieren sie mit den Immunzellen und signalisieren dem Immunsystem, dass von ihnen keine Gefahr ausgeht und eine Abwehrreaktion nicht nötig ist. Die Folge: Die Immunzellen gehen daraufhin in eine Art Ruhezustand und erkennen die Krebszellen nicht mehr als Bedrohung. Die Tumorzellen werden nicht angegriffen und können sich ungestört teilen und der Tumor kann wachsen.37
Doch wie umgeht die Immuntherapie diesen Tarnmechanismus? Sie sorgt für eine Reaktivierung der Körperpolizei bzw. der Immunzellen, damit diese ihre natürlichen Funktionen wieder aufnehmen und sich gegen den Tumor richten können. Dabei werden therapeutische Antikörper, in diesem Fall sogenannte Checkpoint-Hemmer, verwendet. Diese sind passgenau für verschiedene Oberflächenmerkmale auf den Krebszellen beziehungsweise den Immunzellen (T-Zellen) hergestellt. Die Antikörper binden zielgenau an die zu ihnen passenden Checkpoints auf den Zelloberflächen und blockieren sie. Die Immunzellen werden wieder „angeschaltet“, erkennen die Krebszellen wieder als bösartig und greifen sie an.37 Immuntherapien greifen im Gegensatz zu beispielsweise einer Chemotherapie die Krebszellen nicht direkt an, sondern aktivieren die körpereigenen Immunzellen zur Bekämpfung des Tumors. Vor Beginn ist jedoch eine immunhistologische Untersuchung zur Bestimmung des PD-L1-Status notwendig, um zu bestimmen, ob eine Immuntherapie überhaupt wirksam wäre.
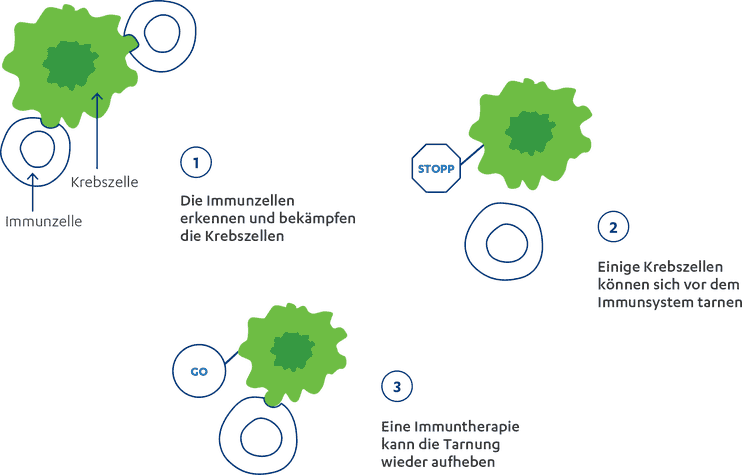
Sie bekommen eine Immuntherapie als Infusion in eine Armvene oder über einen Port verabreicht. Ein Portkatheter oder kurz "Port" ist ein dauerhafter Zugang von außen in eine Vene. Je nach Präparat liegen etwa zwei oder drei Wochen zwischen den Infusionsterminen. Die Infusionsdauer von Immuntherapien ist meist recht kurz, etwa eine halbe bis eine Stunde. Sie können jedoch auch in Kombination mit einer Chemotherapie gegeben werden (Immunchemotherapie). In diesem Fall kommt die Infusionszeit der Chemotherapie noch hinzu, da die Patient:innen die verschiedenen Präparate hintereinander bekommen. In der Regel sind die Infusionen ambulant möglich und Sie können anschließend wieder nach Hause gehen.
Für wen ist eine Immuntherapie geeignet?
Die Immuntherapie greift an sehr speziellen Mechanismen an. Deswegen ist sie auch nicht für jeden gleichermaßen geeignet. Daher prüft der Arzt oder die Ärztin für jeden Patienten und jede Patientin individuell, ob und wenn ja, welche Immuntherapie geeignet ist.
Nebenwirkungen bei einer Immuntherapie können entstehen, wenn das Immunsystem durch die Behandlung übererregt wird.37
Mögliche Nebenwirkungen der Immuntherapie können beispielsweise sein:38
- Anhaltende Erschöpfung (Fatigue)
- Gewichtsverlust
- Übermäßiger Durst oder Appetit, häufiges Wasserlassen
- Übelkeit oder Erbrechen
- Durchfall oder Bauchschmerzen
- Husten
- Kurzatmigkeit
- Fieber
- Hautausschlag, Juckreiz
- Kopfschmerzen, Verwirrtheit
- Muskelschwäche oder -schmerzen
Es ist besonders wichtig, dass Sie Ihr Behandlungsteam zeitnah über neu auftretende oder sich verändernde Symptome oder Nebenwirkungen informieren. Denn es besteht die Gefahr, dass sich das überaktivierte Immunsystem gegen die eigenen Organe richtet und schwere Entzündungen auslöst. Früh erkannt, lassen sich diese Nebenwirkungen gut behandeln oder verhindern.
Ein Film über die Immuntherapie
Schauen Sie sich auch den Film über die Immuntherapie vom SWR aus dem Jahr 2018 an.
Tyrosinkinase-Inhibitoren
Tumorzellen unterscheiden sich von gesunden Körperzellen unter anderem darin, dass sie sich ungebremst teilen. Sie reagieren nicht mehr auf die natürlichen Stoppsignale des Körpers. Die Signalwege, die normalerweise regulieren, wann und wie oft sich eine Zelle teilt, sind bei Krebszellen oft überaktiv. Daher bekommt die Krebszelle ständig das Signal, sich zu teilen. Dies kann zum Beispiel an bestimmten genetischen Veränderungen der Krebszellen liegen. Durch die Identifizierung der genauen Mechanismen konnten Wissenschaftler die Tyrosinkinase-Inhibitoren zielgenau entwickeln, welche diese Signalwege blockieren und so das Tumorwachstum bremsen. Welche Mechanismen in Krebszellen aktiv sind, kann sich von Tumor zu Tumor stark unterscheiden. Um diese zu bestimmen, ist eine vorherige molekulargenetische Untersuchung notwendig. Erst danach kann der Arzt oder die Ärztin festlegen, ob und wenn ja, welche Tyrosinkinase-Inhibitoren infrage kommen. Passend zu Ihrer Mutation erhalten Sie dann den entsprechenden Tyrosinkinase-Inhibitor, wie zum Beispiel einen Inhibitor für die EGFR-, die ALK- oder die ROS1-Tyrosinkinase.
Wie genau wirken Tyrosinkinase-Inhibitoren? Um sich zu teilen, brauchen Zellen ein Signal. Dieses Wachstumssignal nehmen sie in der Regel von außen über Andockstellen (Rezeptoren) auf. Die Rezeptoren leiten das Signal in das Innere der Zellen weiter und lösen dort die Zellteilung aus (1). Für die Signalweiterleitung im Zellinneren sind unter anderem bestimmte Moleküle, sogenannte Tyrosinkinasen, verantwortlich. Das können Sie sich wie einen Telefonanruf vorstellen: Jedes Mal, wenn ein Anruf von außen mit dem Signal „Zellteilung“ kommt, gibt der Empfänger des Anrufs – die Tyrosinkinase – die Nachricht weiter und die Zelle teilt sich. Sind die Tyrosinkinasen dauerhaft aktiviert, bekommen die Zellen ständig das Signal zur Zellteilung – es bilden sich immer mehr Krebszellen und der Tumor wächst.36
Tyrosinkinase-Inhibitoren sind Arzneistoffe, die so klein sind, dass sie ins Innere der Zellen gelangen. Dort setzen sie sich gezielt auf die Tyrosinkinasen und blockieren sie. Sie verhindern also, dass der Empfänger die Nachricht weitergibt (2). Die Tyrosinkinasen können keine Wachstumssignale mehr weiterleiten und die Krebszellen teilen sich nicht mehr und sterben ab.1536
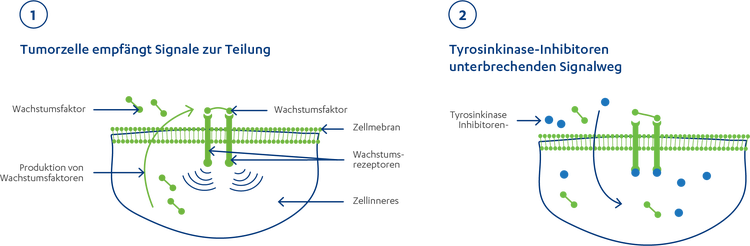
Tyrosinkinase-Inhibitoren gibt es als Tabletten, die Sie zu Hause einnehmen können. Bei Lungenkrebs können beispielsweise EGFR-, ALK-, und ROS1-Mutationen mit Tyrosinkinase-Inhibitoren behandelt werden.15 Diese Therapieoption kann mit anderen Krebstherapien kombiniert werden, wie beispielsweise einem Angiogenese-Inhibitor. Ob und welche Nebenwirkungen auftreten, hängt von dem Präparat ab und ist bei jedem Menschen unterschiedlich.
Folgende Nebenwirkungen könnten Sie bei Tyrosinkinase-Inhibitoren bemerken:39
- Akne-ähnlicher Hautausschlag (Rash)
- Appetitmangel, Gewichtsverlust
- Blutungen im Magen-Darm-Trakt oder Nasenbluten
- Sehstörungen
- Veränderungen des Blutbilds
- Verdauungsbeschwerden wie Übelkeit, Durchfall oder Verstopfung
Wenn Sie eine oder mehrere dieser Nebenwirkungen bei sich feststellen, informieren Sie Ihr Behandlungsteam. Viele Nebenwirkungen der Therapie lassen sich medikamentös gut behandeln.
Zielgerichtete Antikörpertherapie
Antikörper sehen aus wie ein „Y“. Sie können bestimmte Eiweißstrukturen auf Zelloberflächen erkennen und gezielt daran binden. Im Labor können Antikörper hergestellt werden, die mit dem oberen Teil des „Y“ bestimmte Strukturen (z.B. Rezeptoren) auf Tumorzellen erkennen – das macht sich die Krebsmedizin zunutze.
Bei zielgerichteten Antikörpertherapien binden die Antikörper an einen Rezeptor auf der Oberfläche der Tumorzellen, der für das Tumorwachstum wichtig ist. Auf diese Weise kann das Wachstum auf verschiedene Arten gehemmt werden. Durch die Bindung an den Wachstumsrezeptor verhindern Antikörper die Bindung des Wachstumssignals – die Tumorzelle erhält kein Teilungssignal mehr (1). Antikörper können außerdem veranlassen, dass die Wachstumsrezeptoren abgebaut werden und so die Signalkette unterbrechen (2). Zudem können sie mit dem unteren Ende des „Y“ an Immunzellen binden. Tumor- und Immunzellen werden so in eine räumliche Nähe gebracht und die Immunzellen greifen die Tumorzellen an (3).36
Welche Nebenwirkungen auftreten können, hängt vom Medikament ab und ist bei jedem Menschen unterschiedlich. Mögliche Nebenwirkungen sind u. a. Reaktionen der Haut, Verdauungsbeschwerden oder veränderte Blutwerte. Da Antikörpertherapien als Infusion verabreicht werden, können zudem infusionsbedingte Reaktionen auftreten. Diese Nebenwirkungen lassen sich jedoch in den meisten Fällen gut behandeln.36

Angiogenese-Inhibitor
Krebszellen teilen sich häufig und benötigen deswegen viel Energie. Hat der Tumor eine bestimmte Größe erreicht, ist eine eigene Blutversorgung erforderlich, damit er ausreichend Sauerstoff und Nährstoffe bekommt. Um den hohen Energiebedarf des Tumors zu decken, bilden sich neue Blutgefäße zur Versorgung der Krebszellen. Das Wachstum von Blutgefäßen heißt in der Fachsprache „Angiogenese“. Angiogenese-Inhibitoren verhindern die Neubildung von Blutgefäßen.1536
Doch wie wirken Angiogenese-Inhibitoren genau? Ein Tumor kann bestimmte Signale aussenden, um das Wachstum von Blutgefäßen anzuregen. Diese Signale sind sogenannte Wachstumsfaktoren, genauer gesagt Gefäßwachstumsfaktoren (VEGF = vascular endothelial growth factor) (1). Er teilt dem Körper so mit, was er benötigt und der Körper reagiert darauf, indem er neue Blutgefäße bildet und den Tumor so mit Nährstoffen und Sauerstoff versorgt. Um das Wachstum von Blutgefäßen zu verhindern, binden Angiogenese-Inhibitoren an diesen Wachstumsfaktor und blockieren ihn – sie fangen die Signale ab (2). Dadurch kann er Blutgefäßen in der Umgebung des Tumors nicht das Signal übermitteln, weiterzuwachsen und den Tumor zu versorgen. Zusätzlich entwickeln sich bereits vorhandene tumorversorgende Blutgefäße zurück. Die Krebszellen bekommen nicht mehr genügend Sauerstoff und Nährstoffe und sterben ab (3).1536

Sie bekommen Angiogenese-Inhibitoren als Infusion in eine Armvene oder über einen Port verabreicht. Meist liegen drei Wochen zwischen den Terminen. Üblicherweise wird ein Angiogenese-Inhibitor zusammen mit einer Chemotherapie gegeben. Es ist auch möglich, einen Angiogenese-Inhibitor zusammen mit einem Tyrosinkinase-Inhibitor oder einer Immuntherapie zu verordnen. Dabei ergänzen sich die Wirkungen der verschiedenen Präparate. In der Regel kann eine Therapie mit Angiogenese-Inhibitoren so lange verabreicht werden, bis die Krebserkrankung fortschreitet oder der Patient/die Patientin beziehungsweise der behandelnde Arzt/die behandelnde Ärztin die Therapie aufgrund von Nebenwirkungen nicht weiterführen will.
Angiogenese-Inhibitoren können auch außerhalb der Tumorumgebung die Bildung von Blutgefäßen beeinträchtigen. Dadurch kann es zu Blutungen oder Wundheilungsstörungen kommen. Diese Nebenwirkungen treten jedoch nicht bei jedem auf.
Mögliche Nebenwirkungen durch Angiogenese-Inhibitoren können sein:36
- Anhaltende Erschöpfung (Fatigue)
- Appetitlosigkeit und Verdauungsbeschwerden
- Bildung eines Blutgerinnsels (Thrombose)
- Bluthochdruck
- Blutungen, zum Beispiel im Magen-Darm-Trakt
- Veränderungen des Blutbilds
Sollten Sie eine oder mehrere dieser Nebenwirkungen bei sich bemerken, informieren Sie Ihr Behandlungsteam. Die meisten Nebenwirkungen lassen sich medikamentös gut behandeln.
Therapieentscheidung
Die Therapieentscheidung ist ein essenzieller Punkt für die weitere Entwicklung Ihrer Gesundheit. Auch wenn Sie keine Zweifel an der gemeinsam getroffenen Entscheidung haben, können Sie sich trotzdem eine Zweitmeinung von einem anderen Onkologen oder einer anderer Onkologin einholen. Das ist Ihr Recht als Patient:in.


Aufgrund der zahlreichen Behandlungsmöglichkeiten bei Lungenkrebs haben Sie bestimmt die eine oder andere Frage, die Sie im nächsten Beratungsgespräch stellen möchten. Damit Sie keine vergessen, notieren Sie diese am besten direkt. Hier finden Sie eine Checkliste mit Fragen, die auch für Sie interessant sein können. Sie können sich die Liste herunterladen und um eigene Fragen erweitern.
Therapie von Metastasen bei Lungenkrebs
Beim Lungenkarzinom im fortgeschrittenen Stadium können Metastasen in vielen verschiedenen Körperregionen auftreten. Zur Behandlung kommen folgende Therapieoptionen infrage:5
- Hirnmetastasen: stereotaktische Strahlentherapie oder Operation mit adjuvanter Bestrahlung
- Nebennierenmetastasen: Bestrahlung oder Operation
- Knochenmetastasen: Bestrahlung oder Operation
Palliative Tumortherapie
Das primäre Therapieziel in der palliativen Situation ist nicht die Heilung des Lungenkarzinoms. Die palliative Tumortherapie richtet sich gegen die Erkrankung mit dem Ziel, die Lebenserwartung bei fortgeschrittenem Lungenkrebs zu erhöhen. Sie sollen trotz der Erkrankung weiterhin ein möglichst selbstbestimmtes Leben führen können. Denn trotz aller Therapiemöglichkeiten ist Lungenkrebs in einem fortgeschrittenen Stadium in der Regel nicht heilbar, zum Beispiel wenn sich ein Tumor nicht mehr vollständig operativ entfernen lässt oder sich Metastasen gebildet haben. In diesen Fällen steht die palliative Behandlung im Vordergrund. Hierbei kommen beispielsweise Tyrosinkinase-Inhibitoren oder eine Chemotherapie infrage.1
Sprechen die Patient:innen auch auf diese Therapiemöglichkeiten nicht mehr an und haben einen sehr schlechten Allgemeinzustand, dann erhalten sie eine bestmögliche unterstützende Versorgung (best supportive care). Hier steht das Ziel im Vordergrund, Schmerzen zu lindern und eine möglichst gute Lebensqualität zu gewährleisten.
Im Gegensatz zur palliativen Therapie zielt die kurative Therapie auf Heilung ab.
Eine Palliativtherapie umfasst verschiedene Behandlungsmethoden. Dazu gehören sowohl medikamentöse Ansätze wie Schmerzmittel als auch nicht-medikamentöse Optionen wie Atem- und Physiotherapie zur Atemerleichterung.5 Außerdem können Sie auch Angebote von Pflegediensten in Anspruch nehmen und sich beispielweise bei der Körperpflege oder dem Haushalt unterstützen lassen. Eine weitere Möglichkeit sind eine psychoonkologische Begleitung oder psychosoziale Beratungsangebote. Weitere Informationen zur Palliativmedizin finden Sie in der Patientenleitlinie.

Sabine, die aufgrund ihres Lungenkrebses palliativ behandelt wird, gibt in dieser Folge wertvolle Einblicke in ihr Leben mit der unheilbaren Erkrankung und worauf es für sie im Umgang damit ankommt.
Therapie bei einem rezidivierten Lungenkrebs
Bei einem erneuten Auftreten des Bronchialkarzinoms spricht man von einem Rezidiv. Besonders bei spät entdeckten Tumoren kann es zu Rückfällen kommen.40 In den ersten beiden Jahren ist das Risiko für ein Rezidiv am größten.
Die Behandlung richtet sich nach dem Allgemeinzustand, eventuellen genetischen Veränderungen der Krebszellen sowie den bisherigen Therapien. Wenn Sie beispielsweise noch keine Immuntherapie erhalten haben, könnte diese Behandlungsform für Sie infrage kommen. Weitere Möglichkeiten sind Angiogenese-Inhibitoren, Tyrosinkinase-Inhibitoren, eine Kombination aus einer zielgerichteten Therapie mit einer Chemotherapie oder eine alleinige Chemotherapie.1
Patientenleitlinie
Weitere patientengerecht aufbereitete Informationen zum NSCLC und seiner Therapie finden Sie in der Patientenleitlinie NSCLC.
Komplementärmedizin
Zusätzlich zur Schulmedizin können alternative Therapien als ergänzende Maßnahmen bei einer Krebsbehandlung zum Einsatz kommen. Diese stammen teils aus der Naturheilkunde und umfassen auch verschiedene Entspannungstechniken. Sie können die konventionellen Therapien nicht ersetzen, aber sie unterstützen und können Ihnen dabei helfen, Ihr Wohlbefinden zu steigern. Wichtig hierbei ist jedoch, dass Sie vor Beginn einer komplementären Behandlung Ihren Arzt oder Ihre Ärztin darüber informieren und mit ihm besprechen, ob eventuelle Wechselwirkungen oder negative Einflüsse für Ihre schulmedizinische Behandlung entstehen können.
Informieren Sie immer Ihr Behandlungsteam, falls Sie ergänzende Therapiemethoden anwenden möchten.
Nachsorge bei Lungenkrebs
Nach einer Krebstherapie sollten Sie regelmäßig zu Nachsorgeuntersuchungen gehen. Diese Kontrollen helfen dabei, ein mögliches Rezidiv oder Fortschreiten der Erkrankung frühzeitig zu erkennen und eine geeignete Therapie einzuleiten. Zu den Kontrolluntersuchungen gehören neben der Anamnese und einer körperlichen Untersuchung auch ein CT des Brustkorbs und ein Lungenfunktionstest.15 Ein Nachsorgepass kann Ihnen dabei helfen, den Überblick über Nachsorgetermine etc. nicht zu verlieren. Infomaterialien wie einen Nachsorgepass können Sie bestellen oder als PDF herunterladen.
Zusätzlich besteht die Möglichkeit einer Rehabilitation, kurz Reha. Diese kann ambulant oder stationär durchgeführt werden und zum Beispiel medizinisch oder beruflich sein. Bei einer medizinischen Reha lernen Sie beispielsweise, mit welchen Atem- und Physiotherapieübungen Sie Ihre Lunge und Ihren Brustkorb stärken können. Zudem können Sie eine psychologische Betreuung erhalten. Die berufliche Reha hilft Ihnen dabei, wieder an Ihren Arbeitsplatz zurückzukehren oder eine neue Stelle zu finden, falls Sie Ihren alten Beruf nicht mehr ausüben können.41
Aktuelle Forschung
In keiner anderen Krebsart gab es in den letzten zehn Jahren so viele neue Therapiemöglichkeiten wie bei Lungenkrebs. Stetig wird an den Ursachen von Lungenkrebs und neuen Therapieoptionen geforscht. Denn je besser die Eigenschaften eines Tumors bekannt sind, desto genauer kann die Therapie angepasst werden. Doch nicht nur an den neuen, zielgerichteten Therapien wird geforscht, auch Strahlen- und Chemotherapie sind Inhalt einiger Studien.42
Klinische Studien sind auch eine Option für Lungenkrebs-Patient:innen, bei denen die bisher erforschten und zugelassenen Therapien nicht mehr wirken. Im Rahmen einer neuen Studie können sie so mit neuen Medikamenten therapiert werden und ihre Prognose verbessern.
Klinische Studien
Wenn Sie Interesse an klinischen Studien haben, finden Sie hier mehr Informationen dazu: Clinical Trials und bei uns unter Forschung und Entwicklung.
Leben mit Lungenkrebs
Die Diagnose „Lungenkrebs“ soll kein Hindernis sein – egal ob der Krebs in einem frühen Stadium entdeckt wird und potenziell heilbar ist oder ob die Diagnose erst in einem fortgeschrittenen Stadium erfolgt und der Krebs Sie den Rest Ihres Lebens begleiten wird. Das Wichtigste ist, dass Ihre persönliche Lebensqualität so weit wie möglich erhalten bleibt und Sie weiterhin das tun können, was Sie sich vornehmen. Dazu können Sie selbst – neben der Therapie – auch einiges beitragen. Erfahren Sie mehr über den Umgang mit der Diagnose, welche Herausforderungen auf Sie zukommen können und was Sie selbst für eine bessere Lebensqualität tun können.

In dieser Podcast-Folge geht es um eine Krebsdiagnose in der Familie sowie den Umgang mit der neuen Situation. Thomas und seine Frau Dorothea erzählen, wie sie trotz Thomas’ Lungenkrebserkrankung ein erfülltes, glückliches Leben führen und geben wertvolle Tipps für andere Betroffene.
Herausforderungen im Alltag
Sowohl die Krebserkrankung selbst als auch die Nebenwirkungen der Therapie werden sehr wahrscheinlich einen Einfluss auf Ihren Alltag haben. Als betroffene Person haben sie jedoch verschiedene Möglichkeiten, mit diesen Auswirkungen umzugehen, ihnen entgegenzuwirken und so etwas für Ihr persönliches Wohlbefinden zu tun. Schon allein das Wissen, dass Patient:innen selbst etwas tun können, ist für viele hilfreich und motivierend.
Nicht selten erfahren Betroffene Nebenwirkungen ihrer Therapie. Doch die meisten lassen sich mit entsprechenden Medikamenten oder einer Anpassung der Dosis gut behandeln. Sie sollten Ihrem Behandlungsteam (behandelnder Arzt/behandelnde Ärztin, Krankenschwestern/Krankenpflegern oder eventuell vorhandene, speziell geschulte onkologische Pflegekräfte) von den Nebenwirkungen erzählen, denn nur so kann etwas gegen die Nebenwirkungen unternommen werden. Fragen Sie sie auch nach weiteren Tipps, was Sie beispielsweise gegen therapiebedingte Übelkeit unternehmen können.
Aufgrund der Erkrankung und der Behandlung – besonders bei einer operativen Entfernung eines Teils der Lunge – sind viele Betroffene körperlich nicht mehr so fit wie früher. Alltägliche Dinge wie Treppensteigen können zu einer Herausforderung werden. Doch dafür gibt es Hilfsmittel wie beispielsweise einen Treppenlift. Generell können Ihnen verschiedene Hilfsmittel beim Umgang mit der Erkrankung helfen. Wenn Sie zum Beispiel aufgrund einer Chemotherapie an vorrübergehendem Haarausfall leiden, können Sie eine Perücke tragen. Oder haben Sie Beschwerden beim Atmen? Dann können Atemtherapie- oder Sauerstoffgeräte Abhilfe schaffen.43 Sprechen Sie Ihr Behandlungsteam auf mögliche Hilfsmittel an.

Vielleicht mögen Sie im ersten Moment denken, dass Sie bei einer Lungenkrebserkrankung auf Sport oder körperliche Bewegung verzichten sollten. Doch das stimmt nicht. Eine angemessene körperliche Aktivität ist gut für Körper und Seele – egal ob gesund oder erkrankt. Denn Bewegung verbessert nicht nur das Wohlbefinden, sondern erhöht auch die Belastbarkeit. Dabei geht es nicht um eine möglichst hohe Intensität – auch leichte bis moderate körperliche Aktivität hat schon einen positiven Effekt. Beispielsweise können Sie regelmäßig spazieren gehen oder kleinere Fahrradtouren unternehmen. Viele Patient:innen besuchen auch Lungensportgruppen oder machen Physio- oder Atemtherapie. So können Sie Ihre Atemmuskulatur gezielt kräftigen und das Atmen erleichtern. Dabei sollten Sie jedoch stets darauf achten, dass Sie sich nicht überanstrengen. Passen Sie Ihre sportliche Aktivität an Ihre Leistungsfähigkeit an. Am besten besprechen Sie mit Ihrem Arzt oder Ihrer Ärztin, welche Art von Training und wie regelmäßig für Sie passend ist. Der Arzt oder die Ärztin kann Ihnen auch Trainingseinheiten verordnen – dann übernimmt der zuständige Kostenträger bei gesetzlich Versicherten zumindest einen Teil der Kosten.44
Gesund und ausgewogen ernähren sowie viel Obst und Gemüse essen – dieser Tipp gilt für alle Menschen. Haben Sie eine Lungenkrebserkrankung überstanden, kann Ihnen diese Ernährungsweisheit dabei helfen, Ihr Wohlbefinden zu steigern. Sind Sie jedoch gerade mitten in einer Behandlung gilt: Essen Sie, was Ihnen schmeckt und was Sie gut vertragen. Denn häufige Nebenwirkungen einer Lungenkrebstherapie sind Appetitlosigkeit, Übelkeit und Gewichtsverlust. Dann ist das Wichtigste, dass Sie wieder Kräfte sammeln und Ihr Gewicht halten – oder eventuell sogar etwas zunehmen. Das geht am besten mit Lebensmitteln, die Sie gerne essen. Gegebenenfalls kann Ihr Arzt/Ihre Ärztin Ihnen zusätzlich hochkalorische Zusatznahrung verschreiben. Auch eine Ernährungsberatung kann Ihnen weiterhelfen und Tipps für eine kalorienreiche, ausgewogene und trotzdem abwechslungsreiche Zubereitung geben. Aber Vorsicht: Es gibt keine Krebsdiät! Bei solchen Angeboten sollten Sie stets vorsichtig sein und eine eventuelle Ernährungsumstellung immer zuerst mit Ihrem Arzt/Ihrer Ärztin besprechen.44 Hier erfahren Sie mehr zum Thema „Ernährung und Krebs“.
Zusätzlich können Sie ihr Wohlbefinden durch gezielte Entspannungs- und Achtsamkeitsübungen, Yoga oder Mediation steigern. Diese Techniken können beispielsweise gegen Erschöpfung (Fatigue), Ängste oder Niedergeschlagenheit helfen. Auch Akupunktur oder Akupressur helfen einigen Patient:innen bei machen Symptomen.44 Sprechen Sie Ihr Behandlungsteam für mehr Informationen an.
Entdecken Sie, wie spezielle Ernährungsstrategien das Wohlbefinden bei Krebs verbessern können. Praktische Tipps und angepasste Ernährungsempfehlungen warten auf Sie.
Psychische Herausforderungen
Krebs – diese Diagnose versetzt Betroffene und Angehörige häufig zunächst unter Schock. Man fragt sich, wie es jetzt weitergeht: Wie sehen die Therapiemöglichkeiten aus? Wie hoch sind die Heilungschancen? Was ist, wenn der Krebs zurückkommt? Es können Ängste und Sorgen entstehen, mit denen Sie vielleicht allein nicht zurecht kommen. Doch das müssen Sie auch nicht: Suchen Sie sich Unterstützung im Umgang mit Krebs bei Familie und Freunden oder auch bei einer professionellen Stelle. Wenn Sie noch im Krankenhaus sind, können Sie sich an den Kliniksozialdienst wenden. Danach können Ihnen Krebsberatungsstellen oder Psychoonkolog:innen zur Seite stehen. Diese sind spezialisiert auf Menschen mit einer Krebserkrankung und helfen Ihnen, mit Ihren Sorgen und Ängsten besser umzugehen und sie zu verarbeiten.
Zudem können Selbsthilfegruppen, Patientenorganisationen oder andere Verbände für Krebskranke beim Umgang mit der Erkrankung ebenfalls eine große Rolle spielen und die Betroffenen unterstützen. Der Austausch mit anderen Betroffenen gibt Mut und Sie können von den Erfahrungen der anderen profitieren und sich Tipps holen. Hier finden Sie einige nützliche Links:
Bundesverband Lungenkrebs
zielGENau e. V. – Patienten-Netzwerk für Personalisierte Lungenkrebstherapie
Mein Krebsratgeber – Patientenaustausch
Liste verschiedener Patientenorganisationen
Beratungsstellensuche
Psychoonkologensuche
NAKOS
Deutsche Krebshilfe
Deutsche Gesellschaft für Palliativmedizin
INKA – das Informationsnetz für Krebspatienten und Angehörige
Sozialrechtliche Themen
Nach einer Krebsdiagnose haben Sie vermutlich nicht viel Lust, sich mit sozialrechtlichen Themen auseinanderzusetzen. Doch auch das gehört dazu – holen Sie sich hierbei Unterstützung von Familie und Freunden, sie helfen sicher gern. Je früher Sie sich um gewisse Dinge kümmern, desto nahtloser sind die Übergänge, beispielsweise zwischen Therapie und Reha. Informieren Sie sich bei uns über Patientenrechte und Sozialleistungen.
Nach einer Behandlung haben Sie die Möglichkeit einer medizinischen Rehabilitation. Sie kann sowohl ambulant als auch stationär durchgeführt werden. Ziel dabei ist es, Ihren Gesundheitszustand zu erhalten oder zu verbessern.45 Ergänzende Leistungen einer medizinischen Rehabilitation können beispielsweise auch finanzielle Unterstützung für Haushaltshilfen oder Pflegeleistungen sein. Weitere Informationen zu den einzelnen Leistungen erhalten Sie von Ihrem Rehabilitationsträger. Zur Orientierung können Sie die Übersicht der Pflegestützpunkte in Deutschland nutzen.
Neben der medizinischen Reha haben Sie auch ein Anrecht auf eine berufliche Reha. Dabei geht es zum Beispiel darum, wann, wie und in welchem Umfang Sie wieder in Ihren alten Beruf einsteigen können oder ob Sie eine Umschulung machen möchten oder müssen. Hilfreiche Informationen dazu, stehen Ihnen in der Rubrik Beruf und Krebs zur Verfügung. Bei einem Wiedereinstieg können Sie gemeinsam mit Ihrem Arzt oder Ihrer Ärztin und Ihrem Chef oder Ihrer Chefin einen sogenannten Wiedereingliederungsplan erstellen, der sich nach Ihrem Heilungsfortschritt und Leistungsvermögen richtet. Sind Sie nach einer Lungenkrebserkrankung jedoch nicht mehr in der Lage, einer vollen Stelle nachzugehen, können Sie im Rahmen der beruflichen Reha unter anderem auch eine (teilweise) Erwerbsminderungsrente beantragen. Weitere Informationen dazu erhalten Sie bei Ihrem Rehabilitationsträger.46
Aufgrund einer teilweisen Entfernung der Lunge und der damit einhergehenden eingeschränkten Lungenfunktion haben Sie ein Anrecht auf einen Schwerbehindertenausweis. Dadurch haben Sie die Möglichkeit, verschiedene Nachteilsausgleiche in Anspruch zu nehmen. Dazu gehört beispielsweise ein besonderer Kündigungsschutz auf der Arbeit oder Sie können außergewöhnliche finanzielle Belastungen, die durch die Erkrankung entstanden sind, von der Steuer absetzen.47
Es ist ratsam – auch wenn es schwerfällt – dass Sie sich mit den Themen Vorsorgevollmacht, Patienten- und Betreuungsverfügung sowie Testament beschäftigen. Legen Sie rechtzeitig fest, was im Fall der Fälle zu tun ist. Das hilft nicht nur Ihnen, sondern auch Ihren Angehörigen, wenn schwierige Entscheidungen getroffen werden müssen. Anhand von Informationen und Vorlagen zum Thema Vorsorge und Betreuungsrecht können Sie Ihre persönlichen Vorsorgedokumente erstellen. Dafür können Sie auch Ihre Familie oder sonstige Vertraute um Hilfe bitten oder sich professionelle Unterstützung suchen.
Weitere Informationen und nützliche Adressen zu sozialrechtlichen Themen finden Sie auf der Webseite der Krebsgesellschaft.
Tipps für Angehörige
Nicht nur Lungenkrebs-Patient:innen selbst, sondern auch deren Angehörige sind von der Krebsdiagnose betroffen, die auch ihr Leben verändern kann. Sie leiden mit der betroffenen Person, haben Angst um sie und wissen nicht immer, wie sie sich verhalten sollen. Dürfen sie ihre Sorgen zeigen oder müssen sie stark sein? Möchte die betroffene Person über ihre Erkrankung sprechen oder lieber in Ruhe gelassen werden? Möchte sie Hilfe und Unterstützung oder lieber alles selbst erledigen, weil sie niemandem zur Last fallen möchte? In solchen Fällen hilft eine ehrliche Kommunikation. Angehörige sollten die betroffene Person offen fragen, was sie sich wünscht – auch wenn es im ersten Moment unangenehm scheint. Doch nur so können Missverständnisse und unnötige Probleme vermieden werden.48

Oft müssen auch Aufgaben im Alltag neu verteilt werden. Dabei sollten Angehörige aber darauf achten, dass sie sich selbst nicht zu viel zumuten und sich überfordern. Auch Angehörige sollten auf ihre Gesundheit achten und sich gegebenenfalls (professionelle) Unterstützung holen. Sei es durch weitere Familienmitglieder oder Freunde oder bei einer Selbsthilfegruppe oder Beratungsstelle. Denn nur wer selbst physisch und psychisch fit ist, kann anderen helfen.48

Dieser Text entspricht den redaktionellen Standards der JanssenWithMe und wurde von einem Mitglied des redaktionellen Beirats der JanssenWithMe geprüft. Lernen Sie hier den medizinischen Beirat unserer Redaktion kennen.
EM-150081


